คุณสมบัติทางเคมี. อะโรมาติกไฮโดรคาร์บอน
ปฏิกิริยากลุ่มแรกคือปฏิกิริยาทดแทน เราบอกว่าเอรีนไม่มีพันธะหลายพันธะในโครงสร้างของโมเลกุล แต่มีระบบคอนจูเกตที่ประกอบด้วยอิเล็กตรอน 6 ตัว ซึ่งมีความเสถียรมากและให้ความแข็งแรงเพิ่มเติมแก่วงแหวนเบนซีน ดังนั้นในปฏิกิริยาเคมี การแทนที่อะตอมไฮโดรเจนจึงเกิดขึ้นก่อน ไม่ใช่การทำลายวงแหวนเบนซีน
เราเคยพบปฏิกิริยาทดแทนเมื่อพูดถึงอัลเคนแล้ว แต่สำหรับปฏิกิริยาเหล่านี้ ปฏิกิริยาเหล่านี้ดำเนินไปตามกลไกที่รุนแรงและสำหรับเอรีน กลไกไอออนปฏิกิริยาการทดแทน
อันดับแรกฮาโลเจนคุณสมบัติทางเคมี การแทนที่อะตอมไฮโดรเจนด้วยอะตอมฮาโลเจน คลอรีน หรือโบรมีน
ปฏิกิริยาเกิดขึ้นเมื่อถูกความร้อนและมีส่วนร่วมของตัวเร่งปฏิกิริยาเสมอ ในกรณีของคลอรีน อาจเป็นอะลูมิเนียมคลอไรด์ หรือเฟอร์ริกคลอไรด์สาม ตัวเร่งปฏิกิริยาโพลาไรซ์โมเลกุลฮาโลเจน ทำให้เกิดความแตกแยกของพันธะเฮเทอโรไลติกและผลิตไอออน
คลอรีนเป็นไอออนที่มีประจุบวกและทำปฏิกิริยากับเบนซีน
หากเกิดปฏิกิริยากับโบรมีน ตัวเร่งปฏิกิริยาคือไอรอนโบรไมด์หรืออะลูมิเนียมโบรไมด์

สิ่งสำคัญคือต้องสังเกตว่าปฏิกิริยานี้เกิดขึ้นกับโมเลกุลโบรมีน ไม่ใช่กับน้ำโบรมีน เบนซินไม่ทำปฏิกิริยากับน้ำโบรมีน
ฮาโลเจนของเบนซีนที่คล้ายคลึงกันมีลักษณะเฉพาะของตัวเอง ในโมเลกุลโทลูอีน หมู่เมทิลเอื้อต่อการแทนที่ในวงแหวน ปฏิกิริยาเพิ่มขึ้น และปฏิกิริยาเกิดขึ้นภายใต้สภาวะที่เบากว่า กล่าวคือ ที่อุณหภูมิห้อง
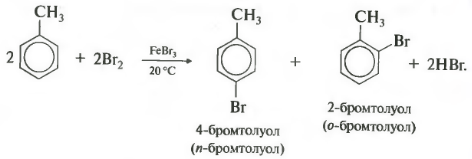
สิ่งสำคัญคือต้องสังเกตว่าการแทนที่จะเกิดขึ้นในตำแหน่งออร์โธและพาราเสมอ ดังนั้นจึงได้ส่วนผสมของไอโซเมอร์
ที่สองคุณสมบัติของไนเตรตของเบนซีน การนำหมู่ไนโตรเข้าไปในวงแหวนเบนซีน
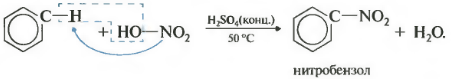
ของเหลวสีเหลืองหนักที่มีกลิ่นอัลมอนด์ขมจะก่อตัวเป็นไนโตรเบนซีน ดังนั้นปฏิกิริยาจึงมีคุณภาพต่อเบนซีน สำหรับไนเตรตจะใช้ส่วนผสมไนเตรตของกรดไนตริกและกรดซัลฟิวริกเข้มข้น ปฏิกิริยาเกิดขึ้นโดยการให้ความร้อน
ฉันขอเตือนคุณว่าสำหรับไนเตรตของอัลเคนในปฏิกิริยา Konovalov จะใช้กรดไนตริกเจือจางโดยไม่ต้องเติมกรดซัลฟิวริก
ในระหว่างการไนเตรตของโทลูอีนตลอดจนระหว่างฮาโลเจนจะเกิดส่วนผสมของออร์โธ - และพารา - ไอโซเมอร์

ที่สามสมบัติอัลคิเลชันของเบนซีนกับฮาโลอัลเคน
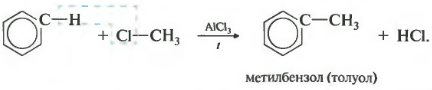
ปฏิกิริยานี้ทำให้เกิดการนำอนุมูลไฮโดรคาร์บอนเข้าไปในวงแหวนเบนซีน และถือได้ว่าเป็นวิธีการผลิตสารคล้ายคลึงกันของเบนซีน อะลูมิเนียมคลอไรด์ใช้เป็นตัวเร่งปฏิกิริยาซึ่งส่งเสริมการสลายตัวของโมเลกุลฮาโลอัลเคนให้เป็นไอออน จำเป็นต้องมีเครื่องทำความร้อนด้วย
ที่สี่สมบัติอัลคิเลชันของเบนซีนกับอัลคีน
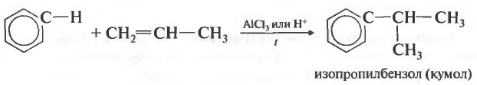
ด้วยวิธีนี้ คุณสามารถได้รับ เช่น คิวมีนหรือเอทิลเบนซีน ตัวเร่งปฏิกิริยาอลูมิเนียมคลอไรด์
2. ปฏิกิริยาเติมเบนซีน
ปฏิกิริยากลุ่มที่สองคือปฏิกิริยาการบวก เราบอกว่าปฏิกิริยาเหล่านี้ไม่ปกติ แต่เกิดขึ้นได้ภายใต้สภาวะที่ค่อนข้างเข้มงวด โดยการทำลายเมฆไพอิเล็กตรอนและการก่อตัวของพันธะซิกมาหกตัว
ประการที่ห้าคุณสมบัติในรายการทั่วไป การเติมไฮโดรเจน การเติมไฮโดรเจน
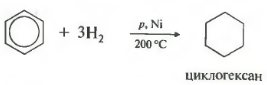
อุณหภูมิ ความดัน ตัวเร่งปฏิกิริยา นิกเกิล หรือแพลทินัม โทลูอีนสามารถทำปฏิกิริยาในลักษณะเดียวกันได้
ที่หกคุณสมบัติคลอรีน โปรดทราบว่า เรากำลังพูดถึงโดยเฉพาะเรื่องปฏิกิริยากับคลอรีน เนื่องจากโบรมีนไม่เกิดปฏิกิริยานี้

ปฏิกิริยานี้เกิดขึ้นภายใต้การฉายรังสีอัลตราไวโอเลตที่รุนแรง Hexachlorocyclohexane หรือชื่ออื่นของ hexachlorane ซึ่งเป็นของแข็งได้ถูกสร้างขึ้น
สิ่งสำคัญคือต้องจำไว้ว่าสำหรับน้ำมันเบนซิน เป็นไปไม่ได้ปฏิกิริยาการเติมของไฮโดรเจนเฮไลด์ (ไฮโดรฮาโลเจน) และการเติมน้ำ (ไฮเดรชั่น)
3. การทดแทนในห่วงโซ่ด้านข้างของสารเบนซีนที่คล้ายคลึงกัน
ปฏิกิริยากลุ่มที่สามเกี่ยวข้องกับความคล้ายคลึงกันของเบนซีนเท่านั้น - นี่คือการทดแทนในห่วงโซ่ด้านข้าง
ที่เจ็ดคุณสมบัติในรายการฮาโลเจนทั่วไปที่อะตอมคาร์บอนอัลฟ่าในสายโซ่ด้านข้าง
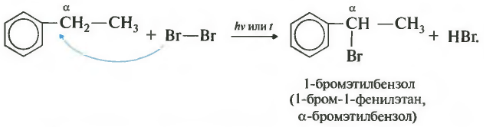
ปฏิกิริยานี้เกิดขึ้นเมื่อถูกความร้อนหรือฉายรังสี และจะเกิดเฉพาะที่อัลฟ่าคาร์บอนเท่านั้น ในขณะที่ฮาโลเจนยังคงดำเนินต่อไป อะตอมฮาโลเจนที่สองจะกลับสู่ตำแหน่งอัลฟา
4. ออกซิเดชันของสารเบนซีนที่คล้ายคลึงกัน
ปฏิกิริยากลุ่มที่สี่คือปฏิกิริยาออกซิเดชัน
วงแหวนเบนซีนแรงเกินไป เบนซีนก็เลย ไม่ออกซิไดซ์โพแทสเซียมเปอร์แมงกาเนตไม่เปลี่ยนสีสารละลาย นี่เป็นสิ่งสำคัญมากที่ต้องจำ
แต่ความคล้ายคลึงกันของเบนซีนจะถูกออกซิไดซ์โดยสารละลายที่เป็นกรดของโพแทสเซียมเปอร์แมงกาเนตเมื่อถูกความร้อน และนี่คือคุณสมบัติทางเคมีประการที่แปด
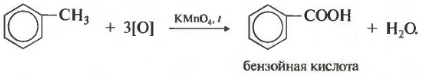
สิ่งนี้จะผลิตกรดเบนโซอิก สังเกตการเปลี่ยนสีของสารละลาย ในกรณีนี้ ไม่ว่าสายโซ่คาร์บอนขององค์ประกอบแทนที่จะยาวแค่ไหน มันก็จะแตกหลังจากอะตอมของคาร์บอนตัวแรกเสมอ และอะตอมอัลฟ่าจะถูกออกซิไดซ์เป็นหมู่คาร์บอกซิลที่มีการก่อตัวของกรดเบนโซอิก ส่วนที่เหลือของโมเลกุลจะถูกออกซิไดซ์เป็นกรดที่เกี่ยวข้อง หรือหากเป็นคาร์บอนเพียงอะตอมเดียว ก็จะเป็นคาร์บอนไดออกไซด์
หากความคล้ายคลึงกันของเบนซีนมีส่วนประกอบของไฮโดรคาร์บอนมากกว่าหนึ่งตัวบนวงแหวนอะโรมาติก การเกิดออกซิเดชันจะเกิดขึ้นตามกฎเดียวกัน - คาร์บอนที่อยู่ในตำแหน่งอัลฟาจะถูกออกซิไดซ์
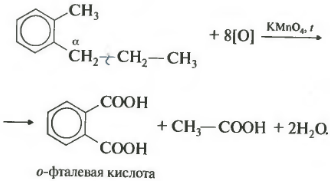
ใน ในตัวอย่างนี้ได้กรดอะโรมาติก dibasic ซึ่งเรียกว่ากรดทาทาลิก
ฉันอยากจะสังเกตการเกิดออกซิเดชันของคิวมีน ไอโซโพรพิลเบนซีน โดยออกซิเจนในบรรยากาศโดยมีกรดซัลฟิวริกอยู่เป็นพิเศษ

นี่เป็นวิธีที่เรียกว่าคิวมีนในการผลิตฟีนอล ตามกฎแล้ว เราพบปฏิกิริยานี้ในเรื่องที่เกี่ยวข้องกับการผลิตฟีนอล นี่เป็นวิธีการทางอุตสาหกรรม
เก้าคุณสมบัติการเผาไหม้, ออกซิเดชันโดยสมบูรณ์กับออกซิเจน เบนซีนและความคล้ายคลึงกันของมันจะเผาไหม้เป็นคาร์บอนไดออกไซด์และน้ำ
ให้เราเขียนสมการการเผาไหม้ของเบนซีนในรูปแบบทั่วไป
ตามกฎการอนุรักษ์มวล ควรมีอะตอมทางด้านซ้ายเท่ากับจำนวนอะตอมทางด้านขวา เพราะในปฏิกิริยาเคมี อะตอมจะไม่หายไป แต่ลำดับของพันธะระหว่างอะตอมนั้นเปลี่ยนแปลงไป ดังนั้นจะมีโมเลกุลคาร์บอนไดออกไซด์มากเท่ากับอะตอมของคาร์บอนในโมเลกุลอารีน เนื่องจากโมเลกุลประกอบด้วยอะตอมของคาร์บอนหนึ่งอะตอม นั่นคือ n CO 2 โมเลกุล จะมีโมเลกุลของน้ำน้อยกว่าอะตอมไฮโดรเจนถึงสองเท่า นั่นคือ (2n-6)/2 ซึ่งหมายถึง n-3
มีจำนวนอะตอมออกซิเจนทางซ้ายและขวาเท่ากัน ทางด้านขวามี 2n จากคาร์บอนไดออกไซด์ เนื่องจากแต่ละโมเลกุลมีอะตอมออกซิเจน 2 อะตอม บวก n-3 จากน้ำ รวมเป็น 3n-3 ทางด้านซ้ายมีจำนวนอะตอมออกซิเจน 3n-3 เท่ากัน ซึ่งหมายความว่ามีโมเลกุลน้อยกว่าสองเท่า เนื่องจากโมเลกุลประกอบด้วยอะตอม 2 อะตอม นั่นคือ (3n-3)/2 โมเลกุลออกซิเจน
ดังนั้นเราจึงได้รวบรวมสมการสำหรับการเผาไหม้ของสารเบนซีนที่คล้ายคลึงกันในรูปแบบทั่วไป
เราขอนำเสนอวิดีโอสอนในหัวข้อ " คุณสมบัติทางเคมีเบนซีน" เมื่อใช้วิดีโอนี้ คุณจะเข้าใจคุณสมบัติทางเคมีของเบนซีน รวมถึงสภาวะที่ไม่เอื้ออำนวยซึ่งจำเป็นสำหรับเบนซีนในการทำปฏิกิริยากับสารอื่นๆ
เรื่อง:อะโรมาติกไฮโดรคาร์บอน
บทเรียน:คุณสมบัติทางเคมีของเบนซีน
ข้าว. 1. โมเลกุลของเบนซีน
เป็นการยากที่จะทำลายเมฆพีอิเล็กตรอนในโมเลกุลเบนซีน ดังนั้นเบนซินจึงเข้าสู่ปฏิกิริยาเคมีน้อยกว่ามากเมื่อเปรียบเทียบกับสารประกอบไม่อิ่มตัว


เพื่อให้เบนซีนเกิดปฏิกิริยาเคมีได้ จำเป็นต้องมีสภาวะที่ค่อนข้างเข้มงวด เช่น อุณหภูมิที่สูงขึ้น และในหลายกรณี ต้องใช้ตัวเร่งปฏิกิริยา ในปฏิกิริยาส่วนใหญ่ วงแหวนเบนซีนที่เสถียรจะยังคงอยู่
1- โบรมีน.

ต้องใช้ตัวเร่งปฏิกิริยา (เหล็ก (III) หรืออะลูมิเนียมโบรไมด์) และไม่อนุญาตให้ใช้น้ำแม้แต่ปริมาณเล็กน้อย บทบาทของตัวเร่งปฏิกิริยาคือโมเลกุลโบรมีนถูกดึงดูดโดยอะตอมโบรมีนตัวใดตัวหนึ่งไปยังอะตอมของเหล็ก เป็นผลให้เกิดขั้ว - อิเล็กตรอนคู่พันธะจะไปที่อะตอมโบรมีนที่เกี่ยวข้องกับเหล็ก:
บ +…. Br - 3 กุมภาพันธ์ .
Br+ เป็นอิเล็กโทรไลต์ชนิดรุนแรง มันถูกดึงดูดไปยังเมฆหกอิเล็กตรอนของวงแหวนเบนซีน และแยกออกจากกันก่อตัวขึ้น พันธะโควาเลนต์โดยมีอะตอมของคาร์บอน:
ไอออนโบรมีนสามารถเข้าร่วมกับไอออนบวกที่เกิดขึ้นได้ แต่การลดลงของระบบอะโรมาติกของวงแหวนเบนซีนนั้นมีประโยชน์มากกว่าการเติมโบรมีนไอออน ดังนั้นโมเลกุลจึงเข้าสู่สถานะเสถียรโดยปล่อยไฮโดรเจนไอออนออกมา:
ปฏิกิริยาการแทนที่อิเล็กโทรฟิลิกทั้งหมดในวงแหวนเบนซีนดำเนินไปโดยกลไกที่คล้ายกัน
2- ไนเตรชัน

เบนซีนและความคล้ายคลึงกันของมันทำปฏิกิริยากับส่วนผสมของกรดซัลฟิวริกเข้มข้นและกรดไนตริก (ส่วนผสมไนเตรต) ในส่วนผสมของไนเตรต ไนตรอนไอออน NO 2 + มีอยู่ในสภาวะสมดุล ซึ่งเป็นอิเล็กโทรฟิล:

3. ซัลโฟเนชั่น
เบนซีนและอารีนอื่น ๆ เมื่อถูกความร้อนจะทำปฏิกิริยากับกรดซัลฟิวริกเข้มข้นหรือโอเลี่ยม - สารละลาย SO 3 ในกรดซัลฟิวริก:

4 - อัลคิเลชันของฟรีเดล-คราฟต์
5. อัลคิเลชันกับอัลคีน

ปฏิกิริยาเหล่านี้ไม่เป็นผลดีอย่างมาก ดังนั้นจะเกิดขึ้นเมื่อได้รับความร้อนหรือถูกฉายรังสีเท่านั้น
1. การเติมไฮโดรเจน
เมื่อได้รับความร้อน ความดันโลหิตสูงและเมื่อมีตัวเร่งปฏิกิริยา Ni, Pt หรือ Pd เบนซินและอารีนอื่นๆ จะเติมไฮโดรเจนเพื่อสร้างไซโคลเฮกเซน:

2- คลอรีนของเบนซีน
ภายใต้อิทธิพลของรังสีอัลตราไวโอเลต เบนซีนจะเติมคลอรีน หากใส่ขวดแก้วควอทซ์ที่มีสารละลายคลอรีนในเบนซีนอยู่ แสงแดดสารละลายจะเปลี่ยนสีอย่างรวดเร็ว คลอรีนจะรวมกับเบนซีน เกิดเป็น 1,2,3,4,5,6-เฮกซะคลอโรไซโคลเฮกเซน ซึ่งเรียกว่า เฮกซะคลอเรน(ก่อนหน้านี้ใช้เป็นยาฆ่าแมลง):

3. การเผาไหม้ของเบนซีน.
เบนซีนและอะโรมาติกไฮโดรคาร์บอนต่างจากอัลเคนตรงที่มีเปลวไฟสว่างและเป็นควัน
สรุปบทเรียน
ในบทเรียนนี้ คุณได้ศึกษาหัวข้อ "คุณสมบัติทางเคมีของเบนซีน" การใช้วัสดุนี้ ทำให้คุณเข้าใจคุณสมบัติทางเคมีของเบนซีน รวมถึงสภาวะที่ไม่เอื้ออำนวยที่จำเป็นสำหรับเบนซีนในการทำปฏิกิริยากับสารอื่นๆ
บรรณานุกรม
1. Rudzitis G.E. เคมี. พื้นฐาน เคมีทั่วไป- เกรด 10: หนังสือเรียนสำหรับ สถาบันการศึกษา: ระดับพื้นฐานของ/ G.E. Rudzitis, F.G. เฟลด์แมน. - ฉบับที่ 14 - อ.: การศึกษา, 2555.
2. เคมี. ชั้นประถมศึกษาปีที่ 10 ระดับโปรไฟล์: หนังสือเรียน เพื่อการศึกษาทั่วไป สถาบัน/ วี.วี. เอเรมิน, N.E. คุซเมนโก, วี.วี. Lunin และคณะ - ม.: อีแร้ง, 2551. - 463 น.
3. เคมี. ชั้นประถมศึกษาปีที่ 11 ระดับโปรไฟล์: วิชาการ เพื่อการศึกษาทั่วไป สถาบัน/ วี.วี. เอเรมิน, N.E. คุซเมนโก, วี.วี. Lunin และคณะ - ม.: อีแร้ง, 2010. - 462 น.
4. Khomchenko G.P. , Khomchenko I.G. รวบรวมปัญหาเคมีสำหรับผู้เข้ามหาวิทยาลัย - ฉบับที่ 4 - อ.: RIA "คลื่นลูกใหม่": ผู้จัดพิมพ์ Umerenkov, 2012. - 278 หน้า
การบ้าน
1. หมายเลข 13, 14 (หน้า 62) Rudzitis G.E., Feldman F.G. เคมี: เคมีอินทรีย์- ชั้นประถมศึกษาปีที่ 10: หนังสือเรียนสำหรับสถาบันการศึกษาทั่วไป: ระดับพื้นฐาน / G. E. Rudzitis, F.G. เฟลด์แมน. - ฉบับที่ 14 - อ.: การศึกษา, 2555.
2. เหตุใดสารประกอบอะโรมาติกจึงมีคุณสมบัติทางเคมีแตกต่างจากไฮโดรคาร์บอนทั้งอิ่มตัวและไม่อิ่มตัว
3. เขียนสมการปฏิกิริยาสำหรับการเผาไหม้ของเอทิลเบนซีนและไซลีน
PRTSVSh (F) สถาบันการศึกษางบประมาณของรัฐบาลกลางด้านการศึกษาวิชาชีพระดับสูง
กรมความปลอดภัยจากอัคคีภัย
ทดสอบ
ในสาขาวิชา “ทฤษฎีการเผาไหม้และการระเบิด”
ภารกิจที่ 1
กำหนดปริมาณและปริมาตรอากาศตามทฤษฎีเฉพาะที่จำเป็นสำหรับการเผาไหม้ไอเบนซีนโดยสมบูรณ์ สภาวะที่อากาศตั้งอยู่นั้นมีลักษณะเฉพาะคืออุณหภูมิ Tb และความดัน Pb และไอระเหยของเบนซีนตามอุณหภูมิ Tg และความดัน Pg แสดงผลการคำนวณในหน่วยต่อไปนี้: ; -
ข้อมูลเริ่มต้น (N - หมายเลขกลุ่ม, n - หมายเลขตามรายชื่อนักเรียน:
ทีวี=300+(-1) ไม่มี *2*N-(-1) n *0.2*n= 277.6 K
Рв=?10 3 =95900 ป่า;
Tg=300?(?1) ยังไม่มีข้อความ ?2?N?(?1) ?0.2?n= 321.6 K;
Рr=?10 3 =79400 ป่า.
С6Н6+7.5О2+7.5?3.76N2=6CO2+3pO+7.5?3.76N2+Qp (1),
โดยที่ QR คือความร้อน ปฏิกิริยาเคมี- จาก สมการที่กำหนดเป็นไปได้ที่จะกำหนดค่าสัมประสิทธิ์ปริมาณสัมพันธ์ของเบนซีนและออกซิเจนโมเลกุล: Vg = 1, V0 = 7.5
2. ปริมาณอากาศตามทฤษฎีเฉพาะ - จำนวนกิโลโมลของอากาศที่จำเป็นสำหรับการเผาไหม้เบนซินหนึ่งกิโลโมลโดยสมบูรณ์ซึ่งคำนวณโดยสูตร:
โดยที่ 4.76 คือปริมาณอากาศที่มีปริมาณออกซิเจนหนึ่งหน่วย = คืออัตราส่วนของสัมประสิทธิ์ปริมาณสัมพันธ์ของออกซิเจนโมเลกุล (Vo) และเบนซิน (Vg)
แทนค่าของ Vo และ Vg เป็น (d) เราจะได้รับ:
3. ปริมาตรอากาศที่จำเป็นสำหรับการเผาไหม้เบนซินหนึ่งกิโลโมลสมบูรณ์ถูกกำหนดดังนี้:
โดยที่ปริมาตรอากาศหนึ่งกิโลโมลที่อุณหภูมิ Тв และความดัน Рв คือที่ไหน ค่าคำนวณโดยใช้สูตร
โดยที่ 22.4 คือปริมาตรโมลาร์ของก๊าซภายใต้สภาวะปกติ Po = 101325 Pa -- ความดันปกติ, To = 273 K คืออุณหภูมิปกติ
แทนที่ TV, To, Pv, Po ลงใน (5) เราจะได้
ปริมาตรอากาศตามทฤษฎีจำเพาะคำนวณโดยใช้สูตร (4):
4. ปริมาตรอากาศที่จำเป็นสำหรับการเผาไหม้ที่สมบูรณ์ของหน่วยปริมาตรของเชื้อเพลิงก๊าซถูกกำหนดดังนี้:
โดยที่ปริมาตรเชื้อเพลิงหนึ่งกิโลโมลคือไอระเหยของเบนซีนที่อุณหภูมิ Tg และความดัน Pg เมื่อพิจารณาแล้วว่า
และการแทนที่ (8) และ (5) ลงใน (7) เราจะได้นิพจน์ต่อไปนี้สำหรับปริมาตรอากาศทางทฤษฎีจำเพาะ:
เราคำนวณค่าของพารามิเตอร์ของกระบวนการเผาไหม้นี้:
ปริมาตรอากาศที่จำเป็นสำหรับการเผาไหม้เบนซิน 1 กิโลกรัมโดยสมบูรณ์ถูกกำหนดดังนี้
มวลโมลของเชื้อเพลิงอยู่ที่ไหน - มวลของเบนซีนหนึ่งกิโลโมลแสดงเป็นกิโลกรัม มวลโมลาร์ของเบนซีนมีตัวเลขเท่ากับน้ำหนักโมเลกุล ซึ่งพบได้จากสูตร:
Ac?nc+An?nn, УiAi?ni (11)
โดยที่ Ac และ An คือน้ำหนักอะตอมของคาร์บอนและไฮโดรเจน nc และ nn คือจำนวนอะตอมของคาร์บอนในโมเลกุลเบนซีน แทนที่ค่า Ac = 12, nc = 6, An = 1, nn = 6 เราได้รับ:
เราค้นหาปริมาตรอากาศตามทฤษฎีเฉพาะโดยการแทนที่ค่า n ในและลงในสูตร (10):
ผลการคำนวณ:
ภารกิจที่ 2
กำหนดปริมาณ ปริมาตร และองค์ประกอบทางทฤษฎีเฉพาะของผลิตภัณฑ์ที่เผาไหม้ด้วยเบนซีน หากทราบค่าสัมประสิทธิ์อากาศส่วนเกิน b อุณหภูมิ Tp และความดัน Pp ของผลิตภัณฑ์ที่เผาไหม้ อุณหภูมิ Tg และความดัน Pg ของไอเบนซีน แสดงผลการคำนวณเป็นเศษส่วนโมล (เปอร์เซ็นต์) และในหน่วยต่อไปนี้: ; -
ข้อมูลเริ่มต้น:
в=1.5+(?1) N ?0.1?N?(?1) n ?0.01?n = 0.2 ;
Рп=?10 3 = 68400 ป่า;
Тп=1600?(?1) N ?20?N?(?1) n ?2?n = 1816 K;
Tg=273?(?1) N ?2?N+(?1) n ?0.2?n = 295.4 K;
Рг=?10 3 = 111600 ป่า;
สารละลาย (N=11, n=2)
1. ขอให้เราเขียนสมการปริมาณสัมพันธ์สำหรับปฏิกิริยาการเผาไหม้ของเบนซีนในอากาศ:
C 6 H 6 +7.5O 2 +7.5?3.76N 2 =6CO 2 +3H 2 O+7.5?3.76N 2 +Qp, (1)
โดยที่ Qp คือความร้อนของปฏิกิริยาเคมี จากสมการนี้ เรากำหนดค่าสัมประสิทธิ์ปริมาณสัมพันธ์ต่อไปนี้:
โวลต์ CO2 =6, โวลต์ pO =3, โวลต์ C6H6 =1, โวลต์ O2 =7.5, โวลต์ N2 =7.5?3.76
2. กำหนดจำนวนผลิตภัณฑ์การเผาไหม้โดยประมาณของเชื้อเพลิงหนึ่งกิโลเมตร:
เราได้รับค่าสัมประสิทธิ์ปริมาณสัมพันธ์ของผลิตภัณฑ์การเผาไหม้และเชื้อเพลิงแทน (2):
3. ปริมาณอากาศตามทฤษฎีเฉพาะ - จำนวนกิโลโมลของอากาศที่จำเป็นสำหรับการเผาไหม้เชื้อเพลิงหนึ่งกิโลโมลโดยสมบูรณ์ถูกกำหนดโดยใช้สูตร:
โดยที่ 4.76 คือปริมาณอากาศที่มีออกซิเจนหนึ่งหน่วย
อัตราส่วนของสัมประสิทธิ์ปริมาณสัมพันธ์ของออกซิเจนโมเลกุลและเบนซีน
แทนที่ค่า (4) V O2 =7.5 และ V C6H6 =1 เราได้รับ:
4. ปริมาณอากาศส่วนเกินต่อเชื้อเพลิง 1 กม. ถูกกำหนดโดยนิพจน์:
อากาศเผาไหม้ด้วยไอน้ำเบนซิน
การแทนที่ค่าในนิพจน์นี้
37,7(0,2-1)=30,16(7)
5. จำนวนรวมของผลิตภัณฑ์การเผาไหม้ต่อหน่วยปริมาณสารเชื้อเพลิงถูกกำหนดโดยผลรวม:
หลังจากแทนค่าแล้วเราได้รับ:
6. เศษส่วนโมลของผลิตภัณฑ์การเผาไหม้ซึ่งแสดงเป็นเปอร์เซ็นต์ถูกกำหนดดังนี้:
ในสูตร (9) สำหรับเศษส่วนโมลของไนโตรเจนและออกซิเจนในผลิตภัณฑ์การเผาไหม้ 0.79 และ 0.21 คือเศษส่วนโมลของสารเหล่านี้ในอากาศ ซึ่งส่วนเกินจะนำไปสู่การเพิ่มสัดส่วนของไนโตรเจนและลักษณะของออกซิเจน ในผลิตภัณฑ์การเผาไหม้
7. ในการกำหนดปริมาตรเฉพาะและผลิตภัณฑ์การเผาไหม้จำเป็นต้องคำนวณปริมาตรโมล - ปริมาตรของก๊าซหนึ่งกิโลโมลภายใต้เงื่อนไขที่ผลิตภัณฑ์ตั้งอยู่:
โดยที่ 22.4 คือปริมาตรของก๊าซหนึ่งกิโลโมลภายใต้สภาวะปกติ T 0 = 273 K คืออุณหภูมิปกติ Po = 101325 Pa คือความดันปกติ
แทนที่ค่า Po, To ลงใน (10) เราได้รับ:
ปริมาตรของผลิตภัณฑ์ที่เกิดขึ้นระหว่างการเผาไหม้เชื้อเพลิงหนึ่งกิโลกรัมโดยไม่คำนึงถึงอากาศส่วนเกินคำนวณได้ดังนี้:
มวลโมลของเชื้อเพลิงอยู่ที่ไหน - มวลของเบนซีนหนึ่งกิโลโมลแสดงเป็นกิโลกรัม มวลโมลของเบนซีนหาได้จากสูตร:
โดยที่ Ac และ An คือน้ำหนักอะตอมของคาร์บอน (12) และไฮโดรเจน (1) n c และ n n คือจำนวนคาร์บอน (6) และไฮโดรเจน (6) อะตอมในโมเลกุลเบนซีน (C 6 H 6)
แทนค่าและใน (12) เราได้
ปริมาตรอากาศส่วนเกินต่อเชื้อเพลิง 1 กิโลกรัม พิจารณาได้ดังนี้
โดยที่ปริมาตรอากาศส่วนเกินหนึ่งกิโลโมลซึ่งเป็นส่วนหนึ่งของผลิตภัณฑ์ที่เผาไหม้คือ เนื่องจากอุณหภูมิและความดันของอากาศส่วนเกินสอดคล้องกับอุณหภูมิและความดันของผลิตภัณฑ์ที่เผาไหม้ ดังนั้น = =220.7
แทนที่ค่านี้เช่นเดียวกับใน (14) เราได้รับ:
ในการคำนวณปริมาตรจำเพาะของผลิตภัณฑ์จากการเผาไหม้เชื้อเพลิงโดยสมบูรณ์ เราจะถือว่าไอระเหยของเบนซีนมีอุณหภูมิ Tg ที่ความดัน:
โดยที่ คือปริมาตรไอน้ำมันเบนซิน 1 กิโลเมตร ที่อุณหภูมิ Tg และความดัน Pg ปริมาตรโมลของเชื้อเพลิงคำนวณโดยใช้สูตร:
แทนที่ค่าผลลัพธ์และค่าดังกล่าวใน (17) เราจะได้รับ:
ปริมาตรอากาศส่วนเกินต่อลูกบาศก์เมตรของไอเบนซีนถูกกำหนดดังนี้:
ทดแทนค่า (20) =30.16 , =และ
ให้ผลลัพธ์ดังต่อไปนี้:
ปริมาตรจำเพาะรวมของผลิตภัณฑ์การเผาไหม้โดยคำนึงถึงอากาศส่วนเกินจะถูกกำหนดโดยผลรวม
ผลการคำนวณ:
XCO2 = %; XH2O = 4.4%; XN2 =%; XO2 =11.7%
เอกสารที่คล้ายกัน
การคำนวณค่าสัมประสิทธิ์การติดไฟของไนโตรเบนซีน C6H5NO2 และคาร์บอนไดซัลไฟด์ CS2 สมการปฏิกิริยาการเผาไหม้ของโพรพิลอะซิเตตในอากาศ การคำนวณปริมาตรอากาศและผลิตภัณฑ์การเผาไหม้ระหว่างการเผาไหม้ของก๊าซไวไฟ การหาจุดวาบไฟของโทลูอีนโดยใช้สูตรของ V. Blinov
ทดสอบเพิ่มเมื่อ 04/08/2017
การคำนวณปริมาตรของอากาศและผลิตภัณฑ์การเผาไหม้ที่เกิดขึ้นระหว่างการเผาไหม้ของสาร สมการปฏิกิริยาการเผาไหม้ของเอทิลีนไกลคอลในอากาศ การเผาไหม้ของส่วนผสมของก๊าซไวไฟ การคำนวณอุณหภูมิการเผาไหม้แบบอะเดียแบติกสำหรับของผสมปริมาณสัมพันธ์ การเผาไหม้ของโพรพานอล
ทดสอบเพิ่มเมื่อ 10/17/2555
ประเภทของการเผาไหม้และพารามิเตอร์หลัก การเปลี่ยนแปลงทางเคมีของเชื้อเพลิงและตัวออกซิไดเซอร์เป็นผลิตภัณฑ์ที่เผาไหม้ สมการของวัสดุและความสมดุลความร้อนของปฏิกิริยาการเผาไหม้ อิทธิพลของค่าสัมประสิทธิ์อากาศส่วนเกินต่อองค์ประกอบของผลิตภัณฑ์การเผาไหม้และอุณหภูมิการเผาไหม้
ทดสอบเพิ่มเมื่อ 17/01/2013
การกำหนดปริมาตรอากาศที่จำเป็นสำหรับการเผาไหม้โดยสมบูรณ์ของมวลหน่วยของสารที่ติดไฟได้ องค์ประกอบของผลิตภัณฑ์การเผาไหม้ต่อมวลหน่วยของสารที่ติดไฟได้ ขีดจำกัดของการแพร่กระจายเปลวไฟของก๊าซ ไอน้ำ และส่วนผสมของฝุ่น-อากาศ ความดันการสลายตัวของการระเบิด
งานหลักสูตร เพิ่มเมื่อ 12/23/2013
การพัฒนามาตรการเพื่อป้องกันการเกิดเพลิงไหม้และการระเบิด การประเมินเงื่อนไขในการพัฒนาและการปราบปราม แนวคิดเรื่องอัตราเหนื่อยหน่าย วิธีการกำหนด ขั้นตอนการเขียนสมการปฏิกิริยาการเผาไหม้ การคำนวณปริมาตรอากาศที่จำเป็นสำหรับการเผาไหม้
งานหลักสูตรเพิ่มเมื่อวันที่ 10/07/2014
การกำหนดองค์ประกอบของผลิตภัณฑ์จากการเผาไหม้ก๊าซโดยสมบูรณ์ การคำนวณอุณหภูมิการเผาไหม้แบบอะเดียแบติกของส่วนผสมก๊าซที่ปริมาตรคงที่และที่ ความดันคงที่- ค่าคงที่จลน์ของปฏิกิริยาการจุดระเบิดในตัวเอง ก๊าซธรรมชาติ- ขีดจำกัดความไวไฟของส่วนผสมของก๊าซ
งานหลักสูตร เพิ่มเมื่อ 19/02/2014
ลักษณะเฉพาะของวิธีการทางอุตสาหกรรมสำหรับอัลคิเลชันของเบนซีนกับโพรพิลีน หลักการของเบนซีนอัลคิเลชันที่มีโอเลฟินส์เข้า เทคโนโลยีเคมี- ปัญหาการออกแบบโรงงานกระบวนการเบนซีนอัลคิเลชัน คำอธิบายของเทคโนโลยีกระบวนการผลิต
วิทยานิพนธ์เพิ่มเมื่อ 11/15/2010
การเผาไหม้เป็นกระบวนการออกซิเดชั่นที่ทรงพลัง ประเภทของการเผาไหม้: การระอุและการเผาไหม้ด้วยเปลวไฟ การระเบิดเป็นกรณีพิเศษของการเผาไหม้ คุณสมบัติทางไฟฟ้าของเปลวไฟ ผลิตภัณฑ์การเผาไหม้ที่หลากหลายอันเป็นผลมาจากการเผาไหม้เชื้อเพลิงที่ไม่สมบูรณ์ การกรองควันผ่านน้ำ
งานทางวิทยาศาสตร์ เพิ่มเมื่อ 29/07/2552
การกำหนดปริมาตรอากาศที่จำเป็นสำหรับการเผาไหม้โพรเพนตามจำนวนที่กำหนดโดยสมบูรณ์ การคำนวณการเปลี่ยนแปลงพลังงานเอนทัลปี เอนโทรปี และกิ๊บส์ โดยใช้ผลที่ตามมาจากกฎของเฮสส์ คำนิยาม มวลฟันกรามเทียบเท่ากับตัวออกซิไดซ์และตัวรีดิวซ์
ทดสอบเพิ่มเมื่อ 02/08/2012
วิธีพิจารณาปริมาณการใช้น้ำมันดูดซับ ความเข้มข้นของเบนซีนในน้ำมันดูดซับที่ออกจากตัวดูดซับ การคำนวณเส้นผ่านศูนย์กลางและความสูงของตัวดูดซับที่บรรจุ การกำหนดพื้นผิวทำความร้อนที่ต้องการในลูกบาศก์คอลัมน์และการไหลของไอน้ำร้อน
อารีน่า - อะโรมาติกไฮโดรคาร์บอนที่มีวงแหวนเบนซีนตั้งแต่หนึ่งวงขึ้นไป วงแหวนเบนซีนประกอบด้วยคาร์บอน 6 อะตอม ซึ่งระหว่างพันธะคู่และพันธะเดี่ยวสลับกัน
สิ่งสำคัญคือต้องสังเกตว่าพันธะคู่ในโมเลกุลเบนซีนไม่คงที่ แต่เคลื่อนที่เป็นวงกลมอยู่ตลอดเวลา
Arenas เรียกอีกอย่างว่าอะโรมาติกไฮโดรคาร์บอน สมาชิกคนแรก ซีรีส์ที่คล้ายคลึงกัน- เบนซิน - C 6 H 6 สูตรทั่วไปซีรีส์ที่คล้ายคลึงกันคือ C n H 2n-6
เป็นเวลานาน สูตรโครงสร้างน้ำมันเบนซินยังคงเป็นปริศนา สูตรที่เสนอโดย Kekule ที่มีพันธะสามสองพันธะไม่สามารถอธิบายความจริงที่ว่าเบนซีนไม่เกิดปฏิกิริยาการเติม ดังที่ได้กล่าวมาแล้วข้างต้นตาม ความคิดที่ทันสมัยพันธะคู่ในโมเลกุลจะเคลื่อนที่ตลอดเวลา ดังนั้นจึงถูกต้องกว่าถ้าดึงออกมาเป็นรูปวงแหวน
เนื่องจากพันธะคู่ในโมเลกุลของเบนซีนจึงเกิดการผันคำกริยา อะตอมของคาร์บอนทั้งหมดอยู่ในสถานะการผสมพันธุ์ sp 2 มุมบอนด์ - 120°
ระบบการตั้งชื่อและไอโซเมอร์ของอารีเนส
ชื่อของ arenes เกิดขึ้นจากการเพิ่มชื่อขององค์ประกอบย่อยลงในสายโซ่หลัก - วงแหวนเบนซีน: เบนซิน, เมทิลเบนซีน (โทลูอีน), เอทิลเบนซีน, โพรพิลเบนซีน ฯลฯ สิ่งทดแทนตามปกติจะแสดงรายการตามลำดับตัวอักษร หากมีองค์ประกอบทดแทนหลายรายการบนวงแหวนเบนซีน ให้เลือก วิธีที่สั้นที่สุดระหว่างพวกเขา.

Arenes มีลักษณะเฉพาะด้วยไอโซเมอร์เชิงโครงสร้างที่เกี่ยวข้องกับตำแหน่งขององค์ประกอบทดแทน ตัวอย่างเช่น สารทดแทนสองตัวบนวงแหวนเบนซีนสามารถอยู่ในตำแหน่งที่ต่างกันได้
ตำแหน่งขององค์ประกอบทดแทนบนวงแหวนเบนซีนนั้นตั้งชื่อตามตำแหน่งที่สัมพันธ์กัน มันถูกแสดงด้วยคำนำหน้า ortho-, meta- และ para ด้านล่างนี้คุณจะพบเคล็ดลับช่วยในการจำเพื่อการจดจำ;)

รับสนามกีฬา
การรับ Arenas มีหลายวิธี:

คุณสมบัติทางเคมีของอารีเนส
Arenes เป็นอะโรมาติกไฮโดรคาร์บอนที่ประกอบด้วยวงแหวนเบนซีนที่มีพันธะคู่คอนจูเกต คุณลักษณะนี้ทำให้ปฏิกิริยาการเติมเกิดขึ้นได้ยาก (แต่ยังเป็นไปได้!)
โปรดจำไว้ว่า เบนซีนและความคล้ายคลึงกันของเบนซีนไม่เหมือนกับสารประกอบไม่อิ่มตัวอื่นๆ ที่ไม่ทำให้น้ำโบรมีนและสารละลายโพแทสเซียมเปอร์แมงกาเนตเปลี่ยนสี

© Bellevich ยูริ Sergeevich 2018-2020
บทความนี้เขียนโดย Yuri Sergeevich Bellevich และเป็นทรัพย์สินทางปัญญาของเขา การคัดลอก การเผยแพร่ (รวมถึงการคัดลอกไปยังเว็บไซต์และแหล่งข้อมูลอื่นบนอินเทอร์เน็ต) หรือการใช้ข้อมูลและวัตถุอื่นใดโดยไม่ได้รับความยินยอมล่วงหน้าจากผู้ถือลิขสิทธิ์มีโทษตามกฎหมาย หากต้องการขอรับเนื้อหาบทความและการอนุญาตให้ใช้ โปรดติดต่อ
